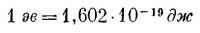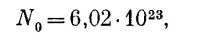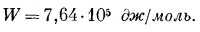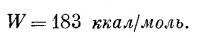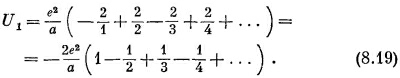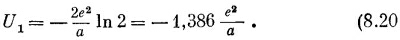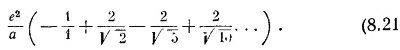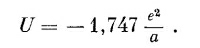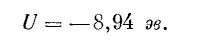| Обучение и материалы |
|---|
| Физический справочник |
| Формулы по физике |
| Шпаргалки по физике |
| Энциклопедия |
| Репетиторы по физике |
| Работа для физиков |
| Быстрый устный счет |
| Виртуальные лабораторные |
| Опыты по физике |
| ЕГЭ онлайн |
| Онлайн тестирование |
| Ученые физики |
| Необъяснимые явления |
| Ваша реклама на сайте |
| Разное |
| Контакты |
| Спецкурс |
|---|
| Фейнмановские лекции |
|
В мире больших скоростей |
Введение в теорию относительности |
|
Лекции по биофизике |
| Лекции по ядерной физике |
| Ускорение времени... |
| Лазеры |
| Нанотехнологии |
| Книги |
| полезное |
|---|
| Смешные анекдоты о физике
Готовые шпоры по физике Физика в жизни Ученые и деньги Нобелевские лауреаты Фото Видео Карта сайта |
| На заметку |
|---|
| Если вам понравился сайт, предлагаем разместить нашу кнопку |
| Дополнительно |
|---|
|
Компьютерные программы по физике 
Физика и юмор 
Онлайн тестирование по физике 
|
Электростатическая энергия ионного кристалла
Рассмотрим теперь применение понятия электростатической энергии в атомной физике. Мы не можем запросто измерять силы, действующие между атомами, но часто нас интересует разница в энергиях двух расстановок атомов (к примеру, энергия химических изменений). Так как атомные силы в основе своей — это силы электрические, то и химическая энергия в главной своей части — это просто электростатическая энергия.
Если наше представление о системе правильно, мы должны уметь проверить его, задав следующий вопрос: сколько понадобится энергии, чтобы разбросать эти ионы, т. е. полностью разделить кристалл на ионы? Эта энергия должна быть равна теплоте испарения соли плюс энергия, требуемая для диссоциации молекул на ионы. Полная энергия разделения NaCl на ионы, как следует из опыта, равна 7,92 эв на молекулу. Пользуясь коэффициентом перевода
и числом Авогадро (количество молекул в грамм-молекуле)
можно представить энергию испарения в виде
Излюбленная единица энергии, которой пользуются физико-химики,— килокалория, равная 4190 дж; так что 1 эв на молекулу — это все равно что 23 ккал/молъ. Химик сказал бы поэтому, что энергия диссоциации NaCl равна
Можем ли мы получить эту химическую энергию теоретически, подсчитывая, сколько работы понадобится для того, чтобы распорошить кристалл? По нашей теории она равна сумме потенциальных энергий всех пар ионов. Проще всего составить себе представление об этой энергии, выбрав какой-то один ион и подсчитав его потенциальную энергию по отношению ко всем прочим ионам. Это даст удвоенную энергию на один ион, потому что энергия принадлежит парам зарядов. Если нам нужна энергия, связанная с одним каким-то ионом, то мы должны взять полусумму. Но на самом деле нам нужна энергия на молекулу, содержащую два иона, так что вычисляемая нами сумма прямо даст нам энергию на молекулу.
Ряд сходится медленно, так что численно его оценить трудно, но известно, что он равен In 2. Значит,
Теперь перейдем к ближайшей линии, примыкающей сверху. Ближайший ион отрицателен и находится на расстоянии а Затем стоят два положительных на расстояниях √2a. Следующая пара — на расстоянии √5a, следующая — на √10a и т. д. Для всей линии получается ряд
Таких линий четыре: выше, ниже, спереди и сзади. Затем имеются четыре линии, которые являются ближайшими по диагонали, и т. д. и т. д.
Это число немного больше того, что было получено в (8.20) для первой линии. Учитывая, что е2/а =–5,12 эв, мы получим
Наш ответ приблизительно на 10% больше экспериментально наблюдаемой энергии. Он показывает, что наше представление о том, что вся решетка скрепляется электрическими кулоновскими силами, в основе своей правильно. Мы впервые получили специфическое свойство макроскопического вещества из наших познаний в атомной физике. Со временем мы добьемся гораздо большего. Область науки, пробующая понять поведение больших масс вещества на языке законов атомного поведения, называется физикой твердого тела. СМОТРИТЕ ТАКЖЕ:Социальные комментарии Cackle |
При использовании материалов сайта ссылка на www.all-fizika.com обязательна.

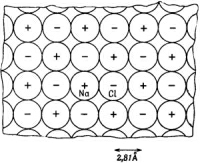 Для первоначального приближения вообразим себе совокупность жестких сфер, представляющих атомы в кристалле соли. Строение такой решетки было определено с помощью дифракции рентгеновских лучей. Эта решетка кубическая — что-то вроде трехмерной шахматной доски. Сечение ее изображено на фиг. 8.5. Промежуток между ионами 2,81 А (или 2,81 ·10-8 см).
Для первоначального приближения вообразим себе совокупность жестких сфер, представляющих атомы в кристалле соли. Строение такой решетки было определено с помощью дифракции рентгеновских лучей. Эта решетка кубическая — что-то вроде трехмерной шахматной доски. Сечение ее изображено на фиг. 8.5. Промежуток между ионами 2,81 А (или 2,81 ·10-8 см).